Angioscanner et rein : risques et prévention chez l'insuffisant rénal
L'angioscanner avec produit de contraste peut fragiliser les reins. Quels patients sont à risque ? Comment se protéger ? Tout ce qu'il faut savoir.
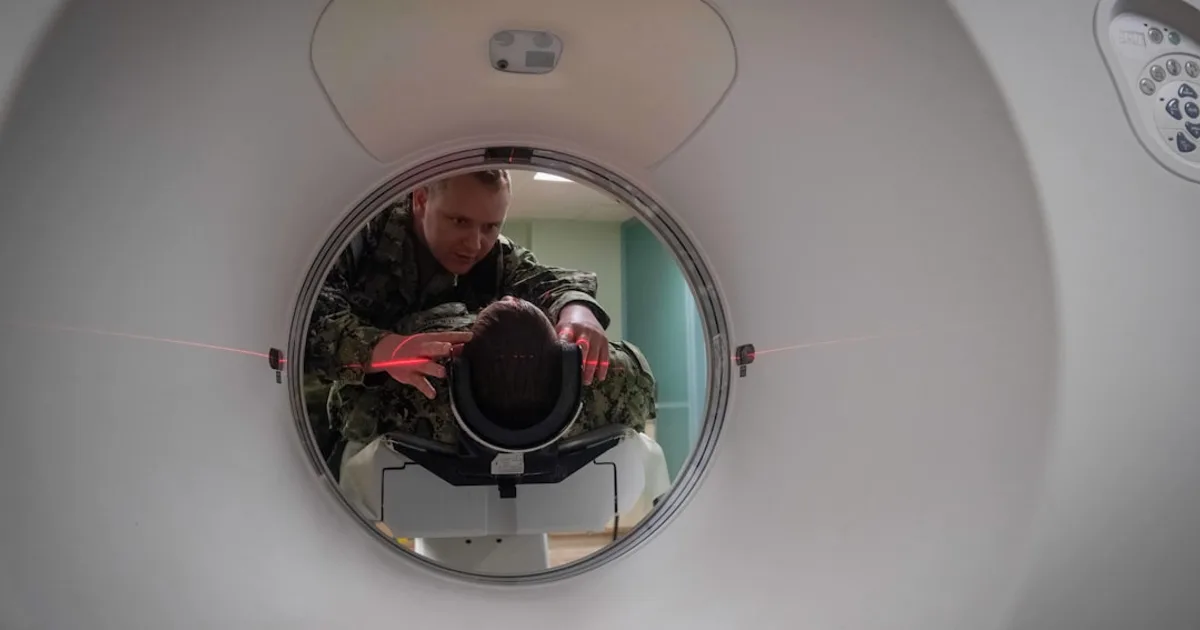
Définition : L’angioscanner (ou tomodensitométrie avec angiographie, CTA) est l’examen d’imagerie de référence en chirurgie vasculaire. Il nécessite l’injection d’un produit de contraste iodé pour visualiser les artères et les veines. Chez les patients présentant une insuffisance rénale, ce produit peut provoquer une dégradation aiguë de la fonction rénale, appelée néphropathie induite par le contraste (NIC) ou, en anglais, contrast-associated acute kidney injury (CA-AKI). Son incidence poolée est estimée à 6,4 % dans une méta-analyse de 40 études, avec des variations importantes selon la fonction rénale de départ.
Qu’est-ce qu’un angioscanner et pourquoi est-il si utilisé ?
L’angioscanner est devenu indispensable dans la prise en charge des maladies vasculaires. Il permet de visualiser avec précision les artères et les veines du corps entier, de détecter un rétrécissement, une obstruction ou une dilatation anormale.
En pratique, il est très souvent prescrit pour les patients atteints d’artérite des membres inférieurs (AOMI) ou d’anévrisme de l’aorte abdominale. Dans ces deux situations, l’angioscanner guide la décision thérapeutique : opérer ou non, et de quelle façon.
Pour les situations d’urgence — embolie pulmonaire, dissection aortique, ischémie aiguë d’un membre — il n’existe souvent pas d’alternative. L’examen est réalisé immédiatement, car le pronostic vital prime.
Comment le produit de contraste peut-il blesser les reins ?
Le produit de contraste iodé est éliminé par les reins. Chez un patient avec des reins en bonne santé, cette élimination se fait sans difficulté. Mais chez un patient dont la fonction rénale est déjà fragilisée, plusieurs mécanismes peuvent conduire à une dégradation aiguë.
Les études identifient trois voies principales [7] :
- Vasoconstriction médullaire : le produit provoque un resserrement des vaisseaux au cœur du rein, créant une hypoxie (manque d’oxygène) dans les cellules rénales les plus sensibles.
- Toxicité tubulaire directe : les cellules des tubules rénaux, chargées de filtrer les déchets, sont agressées directement par les molécules iodées.
- Stress oxydatif : la présence du produit génère des radicaux libres qui endommagent les membranes cellulaires.
Ces trois mécanismes se combinent souvent. Le résultat est une hausse de la créatinine dans le sang dans les 48 à 72 heures suivant l’examen — c’est la signature biologique de la NIC.
Qui est vraiment à risque ?
Tous les patients ne sont pas égaux devant le risque. La fonction rénale de départ est le facteur déterminant.
Le débit de filtration glomérulaire (DFG) — exprimé en mL/min/1,73m² — mesure l’efficacité des reins à filtrer le sang. C’est le chiffre clé que votre médecin examine sur votre bilan sanguin (il figure souvent à côté de la créatinine).
Les études montrent que l’incidence de la NIC varie considérablement selon ce chiffre [6] :
| DFG (mL/min/1,73m²) | Incidence estimée de la NIC |
|---|---|
| 45 – 59 (insuffisance légère) | ~0 % |
| 30 – 44 (insuffisance modérée) | ~2,9 % |
| < 30 (insuffisance sévère) | ~12,1 % |
Au-delà du DFG, d’autres facteurs aggravent le risque [3] :
- Diabète : il multiplie le risque par 3 environ (OR 3,10).
- Volume élevé de produit de contraste : plus la quantité injectée est grande, plus le risque augmente.
- Déshydratation au moment de l’examen.
- Médicaments néphrotoxiques pris en parallèle : anti-inflammatoires non stéroïdiens (ibuprofène, kétoprofène…), aminoglycosides (certains antibiotiques), diurétiques.
Une nuance importante : des études récentes remettent en question l’amplitude de ce risque. Une revue de 2018 n’a pas retrouvé d’augmentation significative de l’insuffisance rénale aiguë ni de la mortalité par rapport à un scanner sans injection [8]. Le risque réel est donc probablement moins dramatique que ce que l’on craignait, mais il reste réel et doit être anticipé, surtout en cas d’insuffisance rénale sévère.
Quelles sont les conséquences possibles ?
Dans la majorité des cas, une NIC est réversible. La fonction rénale revient à son niveau initial en quelques jours.
Mais dans certaines situations, les conséquences peuvent être plus sérieuses [3, 5] :
- Recours à la dialyse temporaire ou permanente : rare en population générale (0,06 % des cas), mais plus fréquent en cas d’insuffisance rénale sévère préexistante.
- Déclin persistant de la fonction rénale : observé dans environ 1,1 % des cas.
- Mortalité accrue : documentée notamment chez les patients avec un DFG inférieur à 30 mL/min/1,73m² [5, 6].
Ces chiffres, bien qu’ils semblent faibles, prennent toute leur importance quand on sait que les patients qui passent le plus d’angioscanners — ceux souffrant d’AOMI sévère ou d’anévrisme — sont précisément les plus susceptibles d’avoir aussi une insuffisance rénale associée, souvent aggravée par le diabète ou l’hypertension.
Comment se protéger : les mesures préventives
C’est la section la plus concrète pour le patient. La bonne nouvelle : des stratégies efficaces existent, et elles sont systématiquement mises en place dans les centres vasculaires.
Ce que fait l’équipe médicale avant l’examen
L’hydratation intraveineuse est la mesure préventive la mieux validée. Elle consiste à perfuser du sérum physiologique à un débit de 1 mL/kg/h pendant 6 à 12 heures avant l’injection, puis pendant 6 à 12 heures après [9]. Cette perfusion dilue le produit de contraste, augmente le débit urinaire et maintient une bonne perfusion rénale.
Le choix du produit de contraste a aussi son importance. Les produits modernes de faible osmolalité ou iso-osmolaires sont nettement moins néphrotoxiques que les agents haute osmolalité utilisés autrefois [9]. Aujourd’hui, les radiologues utilisent systématiquement ces produits de nouvelle génération.
La minimisation du volume injecté est systématiquement recherchée. Des protocoles adaptés permettent de réduire la quantité de contraste tout en conservant une qualité d’image suffisante pour le diagnostic.
L’arrêt temporaire des médicaments à risque est également planifié : anti-inflammatoires, diurétiques, et metformine (antidiabétique oral) sont interrompus avant l’examen selon des protocoles précis.
Le rôle des statines et de la N-acétylcystéine
Les statines à haute dose ont montré un effet protecteur possible sur la fonction rénale en contexte de NIC. Les études suggèrent qu’elles réduisent l’inflammation et le stress oxydatif au niveau rénal [9]. Chez les patients qui en prennent déjà, il est généralement recommandé de les continuer — voire de les introduire en prévention avant un examen à risque.
La N-acétylcystéine (NAC), un antioxydant, a longtemps été proposée en prévention. Mais les preuves de son efficacité restent mitigées [6]. Elle n’est plus recommandée de façon systématique dans les dernières mises à jour.
Ce que le patient peut faire
- Boire suffisamment dans les jours précédant l’examen, sauf contre-indication médicale.
- Signaler tous ses médicaments, y compris ceux pris sans ordonnance (ibuprofène en automédication, par exemple).
- Ne pas interrompre ses traitements sans avis médical — l’arrêt ou la poursuite de chaque médicament doit être décidé avec votre médecin traitant.
- Communiquer ses derniers résultats de créatinine au radiologue avant l’examen.
L’évaluation bénéfice/risque : une décision partagée
Face à un patient insuffisant rénal, la question n’est pas “faut-il éviter l’angioscanner ?” mais “les bénéfices attendus dépassent-ils les risques ?”
En situation d’urgence — dissection aortique, embolie pulmonaire massive, ischémie aiguë des membres — la réponse est toujours oui. La menace pour la vie est immédiate, et le risque rénal est acceptable.
En situation programmée, l’équipe médicale dispose de plusieurs outils :
- Le score de Mehran [4] : un outil de stratification du risque qui combine DFG, présence d’un diabète, état hémodynamique et volume de contraste prévu. Il aide à classer les patients en risque faible, modéré, élevé ou très élevé.
- Les alternatives à l’angioscanner : l’écho-Doppler (sans injection, sans irradiation) est souvent utilisé en première intention pour l’AOMI ou la surveillance d’un anévrisme. L’IRM avec injection de gadolinium est une option, mais elle comporte aussi ses propres risques en cas d’insuffisance rénale sévère (fibrose néphrogénique systémique). Le scanner sans injection est parfois suffisant pour certaines indications.
Cette évaluation est toujours pluridisciplinaire. Le médecin prescripteur (chirurgien vasculaire, cardiologue…), le radiologue et parfois le néphrologue se concertent — surtout quand le DFG est inférieur à 30 mL/min/1,73m².
L’angioscanner vasculaire : une spécificité à connaître
Par rapport à un scanner standard, l’angioscanner injecte souvent des volumes de produit de contraste plus importants. L’opacification des axes artériels — aorte, artères iliaques, artères des membres inférieurs — nécessite un bolus précis et parfois répété. C’est ce qui rend cet examen particulièrement attentif aux protocoles de protection rénale.
Des protocoles ultra-faible dose sont en cours de développement pour les patients à très haut risque. L’objectif est de réduire encore la quantité injectée sans compromettre la qualité diagnostique.
Quand consulter votre médecin ou un spécialiste ?
Consultez votre médecin traitant ou un spécialiste vasculaire ou néphrologue si :
- Votre bilan sanguin montre un DFG inférieur à 45 mL/min/1,73m² et qu’un angioscanner vous est prescrit.
- Vous êtes diabétique et l’examen est programmé à froid (sans urgence).
- Vous prenez des médicaments potentiellement néphrotoxiques et vous n’avez pas reçu d’instructions claires sur leur gestion avant l’examen.
- Vous observez une réduction du volume urinaire, des oedèmes ou une fatigue inhabituelle dans les jours suivant un angioscanner.
- Vous avez des antécédents de réaction au produit de contraste.
Dans la majorité des cas, une bonne préparation permet de réaliser l’angioscanner en toute sécurité. Parlez-en ouvertement avec votre médecin traitant : c’est lui qui connaît l’ensemble de votre dossier médical et qui peut coordonner la prise en charge avec le radiologue et le spécialiste.
Sources :
- Josephson SA et al. Neurology. 2005;64:1805-1806. PMID 15911820. DOI: 10.1212/01.wnl.0000161845.69114.62
- Garfinkle MA et al. AJR. 2015;204:1146-1151. PMID 26001222. DOI: 10.2214/ajr.14.13761
- Kooiman J et al. Méta-analyse. Eur J Radiol. 2012;81:2554-2561. PMID 22177326. DOI: 10.1016/j.ejrad.2011.11.020
- Mehran R et al. N Engl J Med. 2019;380:2146-2155. PMID 31141635. DOI: 10.1056/nejmra1805256
- Mitchell AM et al. Clin J Am Soc Nephrol. 2010;5:4-9. PMID 19965528. DOI: 10.2215/cjn.05200709
- Kim SM et al. Am J Kidney Dis. 2010;55:1018-1025. PMID 20097462. DOI: 10.1053/j.ajkd.2009.10.057
- Zhang F et al. Life Sci. 2020;259:118379. PMID 32890604. DOI: 10.1016/j.lfs.2020.118379
- Patel T, Patel V. Ann Intern Med. 2018;168:JC10. PMID 29335722. DOI: 10.7326/acpjc-2018-168-2-010
- Weisbord SD et al. Essai PRESERVE. N Engl J Med. 2018;378:603-614. PMID 29091581. DOI: 10.1056/NEJMoa1710933
Cet article a été rédigé par le Comité éditorial Petit Veinard et validé sur la base de données publiées dans des revues médicales à comité de lecture. Il ne remplace pas une consultation médicale. Consultez votre médecin traitant ou un spécialiste vasculaire ou néphrologue pour toute question relative à votre santé.
Questions fréquentes
Peut-on faire un angioscanner avec une insuffisance rénale ?
Qu'est-ce que la néphropathie induite par le contraste ?
Faut-il arrêter la metformine avant un angioscanner ?
L'hydratation avant l'angioscanner est-elle vraiment efficace ?
Quand doit-on consulter un néphrologue avant un angioscanner ?
Comité éditorial Petit Veinard
Cet article a été rédigé et validé par des médecins spécialistes en médecine vasculaire. Sources : HAS, ESVS, littérature PubMed.