PRP et ischémie des membres inférieurs : que dit la science ?
Le PRP (Plasma Riche en Plaquettes) peut-il améliorer la cicatrisation en cas d'ischémie des membres inférieurs ? Mécanismes, études cliniques et limites actuelles.
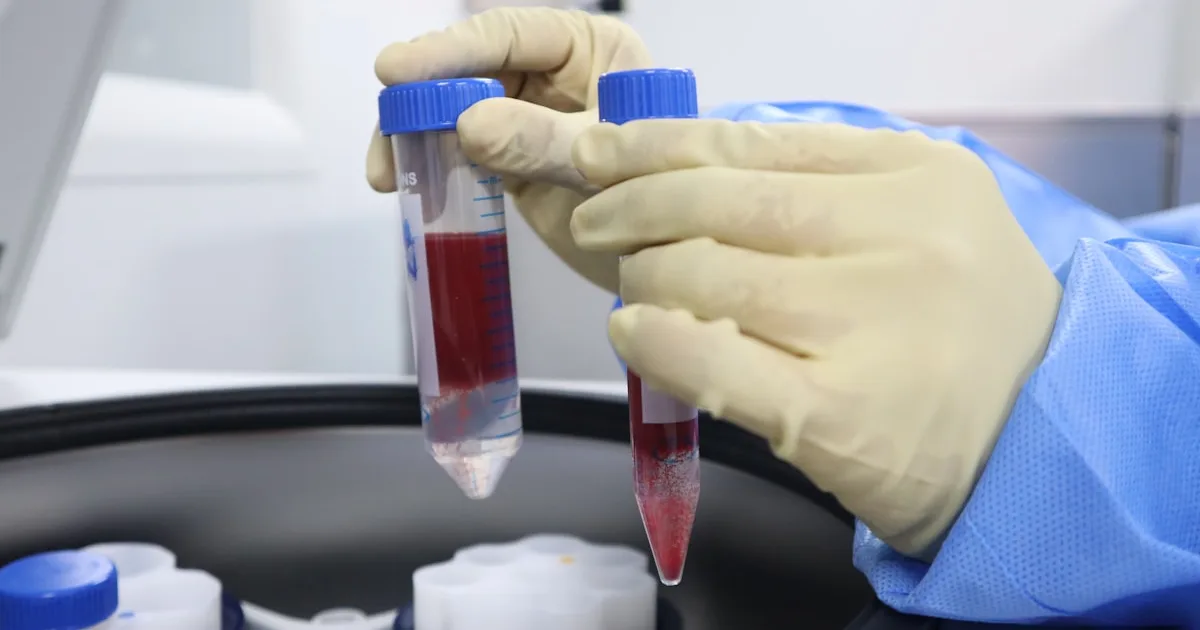
Définition citable : Le PRP (Plasma Riche en Plaquettes, ou Platelet-Rich Plasma en anglais) est un concentré autologue — c’est-à-dire fabriqué à partir du propre sang du patient — obtenu par centrifugation. Il contient entre 2 et 8 fois la concentration habituelle de plaquettes, avec leurs facteurs de croissance associés. Dans le contexte de l’ischémie des membres inférieurs (réduction du flux sanguin artériel vers les jambes, pouvant provoquer des douleurs, des troubles trophiques et des plaies difficiles à cicatriser), le PRP est étudié pour ses propriétés angiogéniques (stimulation de la formation de nouveaux vaisseaux sanguins) et de réparation tissulaire.
Qu’est-ce que le PRP et pourquoi s’y intéresse-t-on dans l’ischémie ?
L’ischémie des membres inférieurs est une conséquence fréquente de l’artérite des jambes (AOMI). Lorsque les artères se bouchent progressivement, les tissus manquent d’oxygène. Dans les cas les plus sévères — on parle d’ischémie critique des membres inférieurs (ICMI) — des plaies apparaissent, douloureuses, qui refusent de cicatriser et peuvent conduire à l’amputation.
La revascularisation (chirurgie ou angioplastie pour rétablir la circulation) reste le traitement de référence. Mais tous les patients ne peuvent pas bénéficier d’une telle intervention. Certains ont des artères trop atteintes, trop fragiles, ou des comorbidités (maladies associées) rendant l’opération trop risquée.
C’est dans ce contexte que les thérapies biologiques, dont le PRP, suscitent un intérêt croissant. L’idée est simple : utiliser les propres ressources biologiques du patient pour stimuler la réparation des tissus lésés et, surtout, favoriser la création de nouveaux vaisseaux sanguins là où la circulation fait défaut.
Mécanismes d’action : comment le PRP agit-il sur les tissus ?
Les plaquettes ne servent pas uniquement à la coagulation. Elles sont de véritables usines à molécules réparatrices, libérant lors de leur activation un arsenal de facteurs de croissance [9, 10] :
- VEGF (Vascular Endothelial Growth Factor) : stimule la formation de nouveaux vaisseaux sanguins — un processus appelé angiogenèse
- PDGF (Platelet-Derived Growth Factor) : favorise la prolifération cellulaire et la réparation des parois vasculaires
- TGF-β (Transforming Growth Factor bêta) : régule la cicatrisation et le remodelage tissulaire
- EGF (Epidermal Growth Factor) : accélère la régénération de l’épiderme (couche superficielle de la peau)
Comme l’ont montré Patzelt et Langer dans une revue publiée dans Current Vascular Pharmacology [9], les plaquettes jouent un rôle central dans l’angiogenèse en libérant ces médiateurs directement sur le site lésé. Martínez et al. ont confirmé dans Frontiers in Physiology [10] que les produits dérivés des plaquettes influencent positivement la réparation tissulaire et la vascularisation.
Imaginez les plaquettes comme des kits de premiers secours biologiques : une fois activées et concentrées en grande quantité dans le tissu blessé, elles envoient des signaux chimiques pour déclencher la réparation et l’irrigation sanguine.
Données précliniques : l’ischémie en modèle animal
L’équipe de Bir et al. a été parmi les premières à étudier les propriétés angiogéniques du PRP à libération prolongée dans un contexte ischémique [1]. Dans leur étude publiée dans le Journal of Vascular Surgery en 2009, ils ont démontré sur un modèle murin (chez la souris) que le PRP formulé pour une libération soutenue de facteurs de croissance favorisait significativement la néovascularisation (formation de nouveaux vaisseaux) dans les tissus ischémiques.
Ces résultats précliniques ont fourni une base biologique solide pour envisager son application chez l’être humain. Ils soulignent également l’importance du mode de délivrance du PRP : une libération progressive des facteurs de croissance semble plus efficace qu’une libération brutale et unique.
Applications cliniques : ce que montrent les études
Plaies ischémiques et ulcères du pied diabétique
Les patients diabétiques sont particulièrement exposés à l’ischémie des membres inférieurs. Le pied diabétique — combinant neuropathie (atteinte des nerfs) et atteinte vasculaire — est une cause majeure d’ulcères chroniques difficiles à cicatriser.
Deux travaux de synthèse font référence dans ce domaine :
- Del Pino-Sedeño et al. ont publié en 2018 dans Wound Repair and Regeneration une méta-analyse portant sur l’utilisation du PRP dans les ulcères du pied diabétique [5]. Leurs résultats montrent que le PRP améliore significativement le taux de fermeture des plaies par rapport aux soins conventionnels seuls.
- Villela et Santos ont mené une revue systématique en 2009 dans Growth Factors [6], confirmant l’intérêt du PRP sur les ulcères diabétiques, tout en soulignant la nécessité d’essais cliniques mieux contrôlés.
Ces données concernent en partie des plaies à composante ischémique. Elles constituent une base d’evidence (niveau de preuve) modéré, suffisant pour justifier l’utilisation du PRP en pratique clinique encadrée, mais pas encore assez robuste pour des recommandations généralisées.
Après revascularisation des membres inférieurs
La revascularisation chirurgicale d’un membre ischémique — pontage artériel ou angioplastie — ne garantit pas toujours une cicatrisation rapide des plaies préexistantes. Les tissus longtemps privés d’oxygène restent fragilisés même après rétablissement de la circulation.
Massara et al. ont étudié l’application de PRP autologue après revascularisation des membres inférieurs dans Seminars in Vascular Surgery [2]. Leurs résultats suggèrent que l’application locale de PRP sur les plaies permet d’accélérer la cicatrisation en phase postopératoire. Cette approche combinée — revascularisation chirurgicale suivie d’application locale de PRP — représente une piste thérapeutique complémentaire prometteuse.
Ulcères veineux chroniques
Si l’ischémie artérielle est la principale indication étudiée, les plaies veineuses bénéficient également de l’action des facteurs plaquettaires. Otero et al. ont présenté en 2018 dans Cytotherapy [3] des données sur la thérapie cellulaire associant PRP autologue dans le traitement d’ulcères veineux chroniques, avec des résultats encourageants sur la réduction de la surface des plaies.
Pour aller plus loin sur les thérapies biologiques appliquées aux ulcères veineux, vous pouvez consulter notre article dédié au PRF et aux ulcères veineux chroniques, qui présente une approche voisine basée sur la fibrine riche en plaquettes.
Ischémie critique : les thérapies cellulaires en appoint
L’étude pilote d’Iafrati et al., publiée dans le Journal of Vascular Surgery en 2012 [4], a évalué les résultats à moyen terme d’un concentré de moelle osseuse — une thérapie cellulaire proche par son principe du PRP — chez des patients en ischémie critique des membres inférieurs. Bien que portant sur une population restreinte, cette étude illustre l’intérêt croissant pour les approches biologiques autologues dans les formes les plus sévères de la maladie, là où les options chirurgicales sont épuisées.
Résultats comparatifs : que peut-on attendre du PRP ?
| Indication | Niveau de preuve | Résultat principal | Limites |
|---|---|---|---|
| Ulcères du pied diabétique | Modéré (méta-analyse) [5] | Meilleur taux de fermeture vs soins standards | Hétérogénéité des protocoles |
| Post-revascularisation | Faible (série de cas) [2] | Cicatrisation accélérée en postopératoire | Effectifs réduits |
| Ulcères veineux chroniques | Faible (données préliminaires) [3] | Réduction de la surface des plaies | Absence d’essai randomisé dédié |
| Ischémie critique (modèle animal) | Préclinique [1] | Néovascularisation significative | Non validé en essai clinique de grande taille |
Limites actuelles : des questions importantes restent ouvertes
Le PRP suscite un enthousiasme justifié, mais les spécialistes rappellent que plusieurs obstacles freinent encore son intégration dans les recommandations officielles.
L’hétérogénéité des protocoles est le premier problème. Il n’existe pas de méthode standardisée pour préparer le PRP : la concentration en plaquettes, le mode d’activation, le volume injecté ou appliqué, le nombre de séances — tout cela varie d’une équipe à l’autre. Comparer les études dans ces conditions est difficile.
La taille des études pose également question. La plupart des essais cliniques disponibles portent sur de petits groupes de patients. Les résultats sont encourageants, mais ils ne permettent pas encore de conclusions définitives sur l’efficacité et la sécurité à long terme.
La variabilité biologique entre patients est un autre facteur. La qualité du PRP préparé dépend directement de l’état des plaquettes du donneur — lui-même influencé par l’âge, les médicaments pris, les maladies associées.
Enfin, les études actuelles portent peu sur l’ischémie critique sévère isolée. La majorité des données concerne les plaies chroniques dans un contexte mixte (artériel et veineux) ou diabétique.
Ce que le PRP ne peut pas faire
Il est important de préciser ce que le PRP ne remplace pas :
- La revascularisation artérielle, qui reste le seul traitement capable de rétablir un flux sanguin suffisant lorsque les artères sont obstruées. Aucune thérapie biologique ne peut se substituer à un pontage ou à une angioplastie si ceux-ci sont possibles.
- Le traitement médical de fond (contrôle des facteurs de risque cardiovasculaires, statines, antiagrégants plaquettaires, arrêt du tabac), indispensable dans toute forme d’AOMI, comme nous l’expliquons dans notre article sur l’artérite des jambes et ses traitements.
- Les soins locaux standards, qui restent la base de la prise en charge des plaies chroniques.
Le PRP est un outil complémentaire, pas un traitement de substitution.
Perspectives : vers une médecine régénérative vasculaire ?
Les thérapies biologiques autologues — PRP, PRF, cellules souches, concentrés de moelle osseuse — représentent un domaine de recherche en plein essor en médecine vasculaire. L’objectif à long terme est de disposer d’outils capables de stimuler la réparation vasculaire et tissulaire là où les méthodes classiques atteignent leurs limites.
Des essais cliniques de plus grande envergure, avec des protocoles standardisés et des critères d’évaluation harmonisés, sont nécessaires pour confirmer la place du PRP dans l’arsenal thérapeutique de l’ischémie des membres inférieurs. Les études en cours augurent de résultats plus définitifs dans les prochaines années.
Quand consulter votre médecin ?
Consultez votre médecin si vous présentez :
- Une plaie au pied ou à la jambe qui ne cicatrise pas en 2 à 4 semaines
- Des douleurs dans les jambes à la marche, disparaissant au repos (claudication intermittente)
- Des douleurs de repos au niveau du pied, surtout la nuit
- Un pied froid, pâle, ou de couleur violacée
Ces symptômes peuvent indiquer une ischémie des membres inférieurs. Un bilan vasculaire rapide est recommandé. Votre médecin pourra vous orienter vers un spécialiste vasculaire pour évaluer si des thérapies complémentaires comme le PRP sont appropriées dans votre situation.
Sources :
- Bir SC et al. J Vasc Surg. 2009;50:870-879. PMID 19700085. DOI: 10.1016/j.jvs.2009.06.016
- Massara M et al. Semin Vasc Surg. 2015;28:195-200. PMID 27046199. DOI: 10.1053/j.semvascsurg.2016.01.002
- Otero GE et al. Essai randomisé de phase 2. Cytotherapy. 2018;20:S117. DOI: 10.1016/j.jcyt.2018.02.348
- Iafrati MD. J Vasc Surg. 2012;56:1482-1483. PMID 23078763. DOI: 10.1016/j.jvs.2012.08.093
- del Pino-Sedeño T et al. Méta-analyse. Wound Repair Regen. 2018;27:170-182. PMID 30320442. DOI: 10.1111/wrr.12690
- Villela DL, Santos VLCG. Revue systématique. Growth Factors. 2009;28:111-116. PMID 20067399. DOI: 10.3109/08977190903468185
- Akgul A et al. Essai randomisé contrôlé. Lymphat Res Biol. 2020;18:439-447. PMID 32286917. DOI: 10.1089/lrb.2019.0064
- Gamal H et al. Cytotherapy. 2018;20:S116. DOI: 10.1016/j.jcyt.2018.02.345
- Patzelt J, Langer HF. Curr Vasc Pharmacol. 2012;10:570-577. PMID 22724471. DOI: 10.2174/157016112801784648
- Martínez CE et al. Front Physiol. 2015;6:290. PMID 26578986. DOI: 10.3389/fphys.2015.00290
Cet article a été rédigé par le Comité éditorial Petit Veinard et validé par des sources scientifiques référencées. Il ne remplace pas une consultation médicale. Consultez votre médecin pour toute question relative à votre santé.
Questions fréquentes
Le PRP peut-il remplacer une opération pour l'ischémie des membres inférieurs ?
Combien de séances de PRP faut-il pour cicatriser une plaie ischémique ?
Le PRP est-il remboursé par l'Assurance Maladie pour l'ischémie des membres inférieurs ?
Quelle est la différence entre le PRP et le PRF ?
Le PRP est-il efficace sur les ulcères du pied diabétique ?
Comité éditorial Petit Veinard
Cet article a été rédigé et validé par des médecins spécialistes en médecine vasculaire. Sources : HAS, ESVS, littérature PubMed.